こんにちは、trans(トランス)です。
今回は、遷移金属錯体の磁化率を測定し、特性を確認する実験について解説いたします。
まず、磁化率の章では、反磁性や常磁性などについて解説をいたします。
次に、測定方法の章では、磁化率の測定方法や磁化率の算出方法について解説いたします。
最後に、遷移金属錯体の章では、3d電子配置などについて解説いたします。
実験の予習をやらなければいけないけど時間が無いという学生に向けて、予習の手間が省けるように、この記事を書いています。スマホを見ながら電車で予習することもできます。実験項目は某大学の実験テキストを参考にしています。
レベル的には、大学の学部生レベルを想定していますが、高校生も化学の発展的なことに興味があれば、読んでみてください。
それでは行きましょう!
1、磁化率

磁場中に物質を置くと、その物質は磁気モーメントを持ちます。その単位当たりの磁気モーメントを磁化といいます。
また、磁化率χは、磁化Mと外部磁場Hの比例関係から以下の式で定義されます。
M=χH…①
このときの磁化率はcgs電磁系において、無次元の物質量として扱われます。
1‐1、反磁性について
反磁性とは、外部磁場を弱める方向に磁化する性質のことです。このときはχ<0であります。
ここで注意すべき点は、反磁性は、外部磁場への電子雲の応答であるから、全ての物質に存在するということです。
また、反磁性磁化率について、以下のパスカルの加成則が成り立ちます。
χ=Σniχi+Σmkλk…②
ni:分子内のi番目の同種原子の個数
χi:構成原子に割り当てられた磁化率
mk:k番目の同種結合の個数
λk:結合の性質に依存する補正項
ここで磁化率χを扱いやすくするために、モル磁化率χmol(磁化率にモル体積をかけたもの、単位:cm3/mol)、グラム磁化率χg(χを密度で割ったもの、または、すなわちχgにモル質量をかけたものがχmol、単位:cm3/g)を定義します。
以下に代表的な原子および原子団の磁化率を示します。
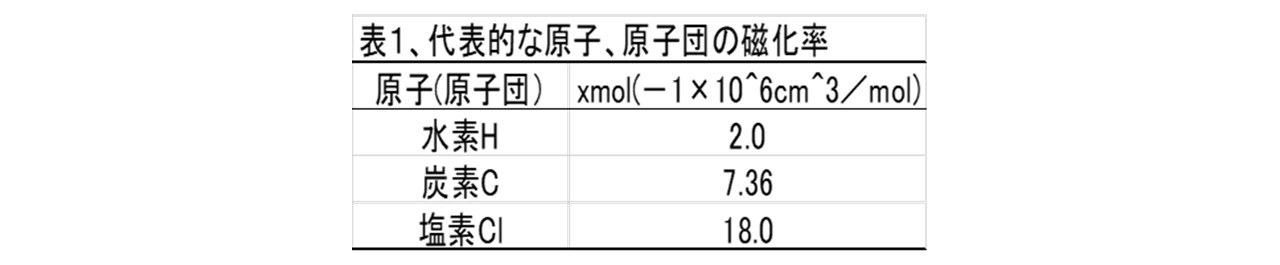
また、結合や原子団に対する補正項は以下の通りです。
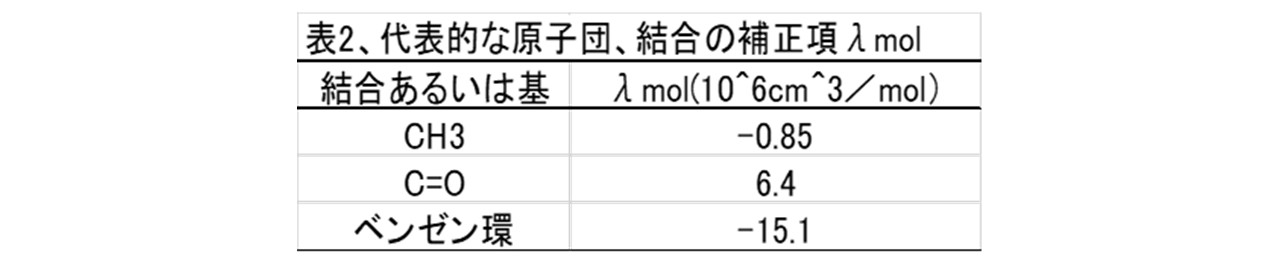
1‐2、常磁性
常磁性とは、磁場中で物質が外部磁場と同じ方向に磁化される性質のことです。このときは、x>0であります。
常磁性は、外部磁場によって磁気モーメントの向きを変えることで生じます。これを永久磁気双極子モーメントといい、これは電子スピンと電子の軌道角運動量が原因で生じます。
このことから全角運動量Jh(-)は、電子スピンSh(-)と軌道角運動量Lh(-)の和であるため、J=S+Lで示されます。
また、磁気モーメントと全角運動量の関係は以下のようになます。
μ=gμBJ…③
μ:磁気モーメント
g:ランデのg因子
μB:ボーア磁子(=eh(-)/2m,m:電子の質量)
J:全角運動量
式③から磁場H中の磁気モーメントのポテンシャルエネルギーは以下のようになります。
-μ・H=-gμBJ・H=-gμBmJH…④
mJ:Jの磁場方向成分
量子力学を用いると、mJは、2J+1通りの値をとります。すなわち、mJ=±J,±(J-1),....,0となります。
熱力学観点から、熱平衡状態にある磁化Mの熱統計平均は、ボルツマン分布を用いると以下のようになります。
M=NgμBΣJmj=-J(mJexp(gμBmJH/kT)/ΣJmj=-J(exp(gμBmJH/kT)…⑤
N:単位面積あたりの個数
T:絶対温度
また、高温状態のときは、gμBmJH≪kTと仮定でき、以下の式が得られます。
M=Ng2μB2HJ(J+1)/3kT…⑥
式⑥を式①に代入すると以下のようになります。
χ=M/H=Ng2μB2J(J+1)/3RT…⑦
式⑦をモル磁化率に換算すると以下のようになります。
χmol=NL2g2μB2J(J+1)/3RT…⑧
NL:ロシュミット数(アボカドロ数と同値)
有効磁気モーメントμeff、有効ボーア磁子数neffを以下のように定義します。
μeff=g(J(J+1))1/2μB=neffμB…⑨
neff=g(J(J+1))1/2…⑩
式⑨を式⑧に代入すると以下のようになります。
χmol=NL2μeff2/3RT=NL2μB2 neff2/3RT…⑪
式⑪から算出した実験的なボーア磁子数nexpは以下の通りです。
nexp=(3RTxmol/NL2μB2)1/2…⑫
磁気モーメントが、電子スピンSh(-)で決まる場合、スピン・オンリーの式が成立するので、L=0すなわち、J=Sと置き換えることができます。また、L=0のときのランデのg因子は2であり、これらのことから、J=S、g=2を式⑩に代入すると以下のようになります。
neff=2(S(S+1))1/2…⑬
さらに、常磁性イオンの不対電子の数をnとすると、S=(1/2)nとなり、この値を式⑬に代入すると以下のようになります。
neff=2(1/2n(1/2n+1))1/2=(n(n+2))1/2…⑭
式⑫と式⑭を比較して、不対電子の数を推測することができます。
1‐3、強磁性と反強磁性
常磁性状態では、各磁気モーメントが孤立しているため、これらの間で相互作用が起きません。
このとき、以下のキュリーの法則が成り立ちます。
χ=C/T…⑮
C=Ng2μB2J(J+1)/3k(キュリー定数)…⑯
一方、磁気モーメント間の相互作用が無視できなくなると、キュリー・ワイスの法則で式⑮が以下のように示されます。
χ=C/(T-θ)…⑰
このθはワイス定数(常磁性キュリー温度)といい、θ>0のときに磁気モーメント間の相互作用が強磁性で、θ<0のときに磁気モーメント間の相互作用が反強磁性です。
強磁性とは、隣り合う磁気モーメントが同方向に並んだ方がエネルギー的に有利であるということで、反強磁性は逆の方向に並んだ方がエネルギー的に有利であることです。
磁気モーメント間の相互作用は、基本無視できますが、温度が十分に低く、磁気相転移温度以下になったときには注意する必要があります。
2、測定方法

ここからは、磁化率の測定方法について解説していきます。
2-1、電子天秤について
本実験では、エバンス法を用いていますが、基本的にはグーイ法に基づいているため、まずグーイ法について説明します。
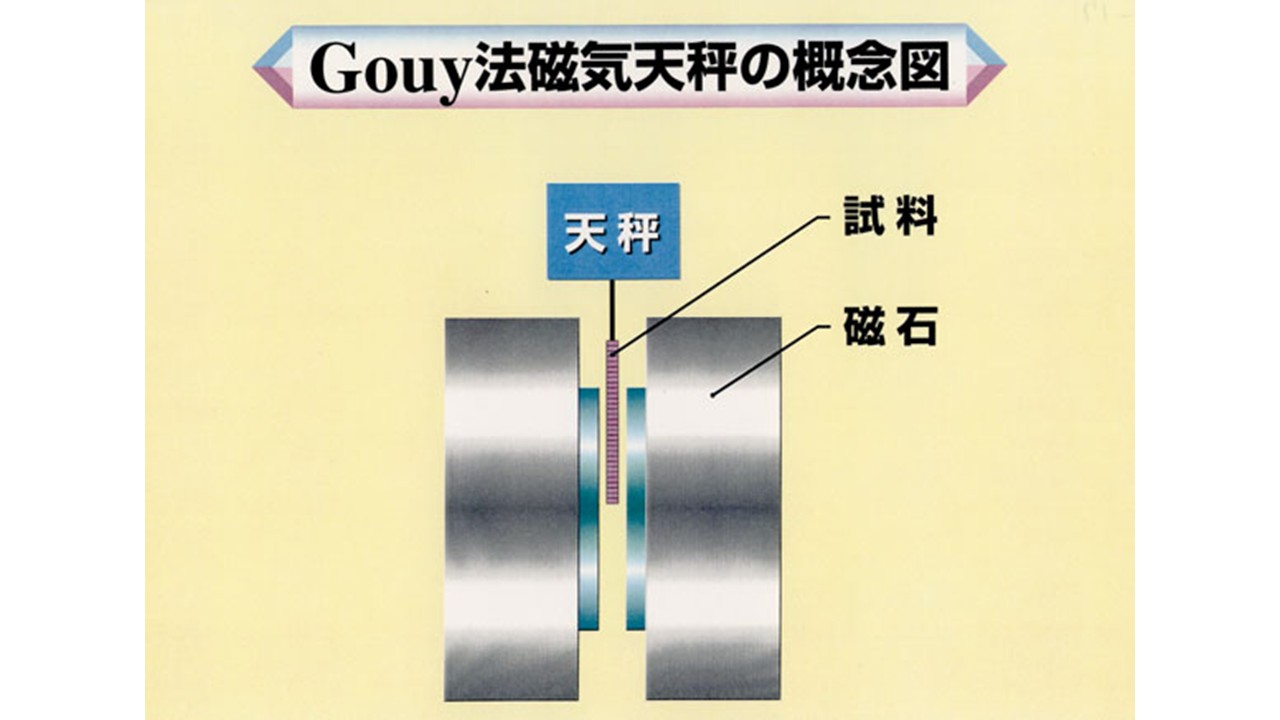
グーイ法による磁化率測定装置は以下のようになっています。
上に示したように、試料管中の試料は下方が均一な強い磁場H0がかかっている領域にあり、上方が強い磁場を受けない領域にあるように天秤につるされています。試料と磁場の相互作用で、縦方向(z軸方向)に試料が力を受けます。
この力は、磁場によって試料の体積Δvで生じた磁気モーメントM(z)Δvが不均一磁場H(z)の中で、磁場勾配によって受ける力M(z)Δv(dH/dz)によるものであります。ここでM(z)は、磁化であるので式①を用いると以下のようになります。
χ=M(z)/H(z)…⑱
ここでz軸上にあり、体積Δvの試料のポテンシャルエネルギーΔA(z)は、Δvをz軸方向に、磁場がないところまで移動するのに必要な仕事の符号を入れ替えたものであるので、以下のように示されます。
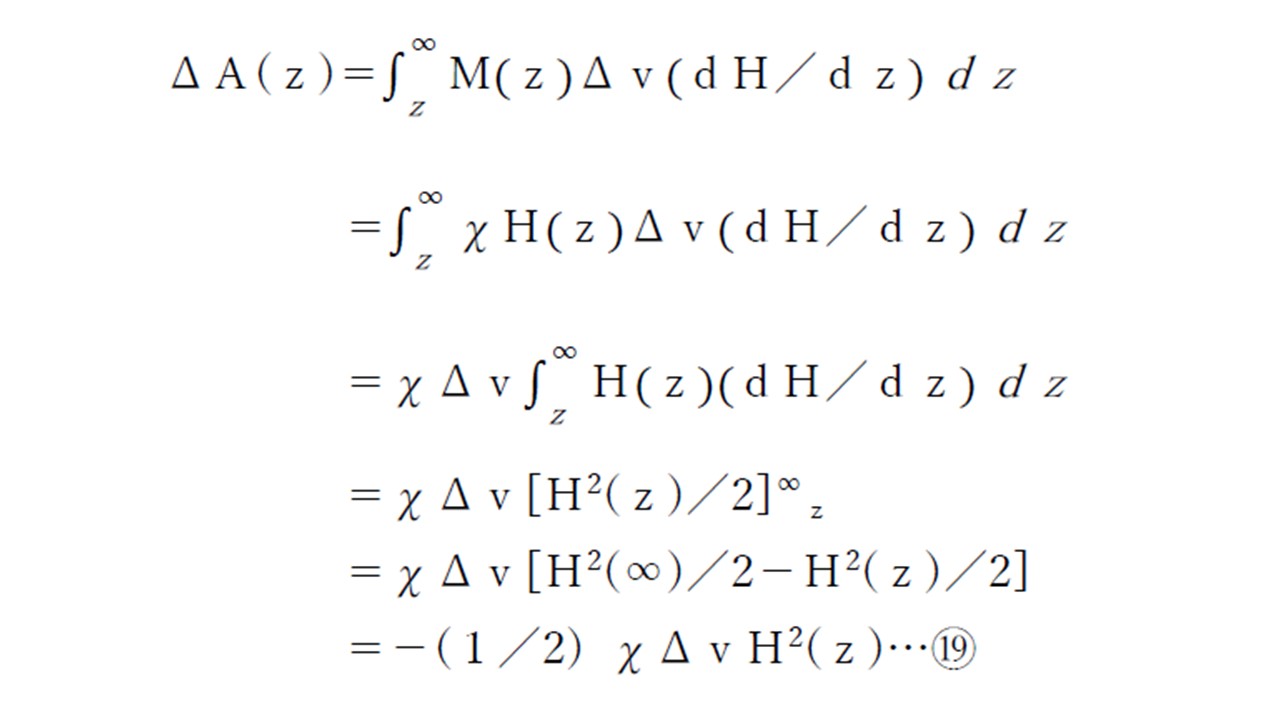
Δvに働く力ΔKは、ポテンシャルエネルギーの勾配の符号を変えたものであるので以下のようになります。
ΔK=-(dΔA(z)/dz)=(1/2)χΔv(dH2(z)/dz)…⑳
また、試料全体に働く力Kは、式⑳を積分すればよいので以下のようになります。

㉒式から分かるように磁場と試料の相互作用による力は、磁化率に比例します。
すなわち、この比例定数-(1/2) aH20を求めれば、未知試料の磁化率を求めることができます。
ここからは、エバンス法について説明いたします。
先ほど述べたグーイ法と基本的に変わりませんが、グーイ法では磁石を固定していたのに対し、エバンス法では試料を固定し、ワイヤーで橋渡しされた2個の磁石の一方により引かれる力を測定します。
ここで得られる力も原理的には、グーイ法と同じであるので、こちらも式㉒の比例定数を求めればよいことが分かります。
2-2、磁化率の算出法
先ほど記したように、式㉒の比例定数-(1/2) aH20を求めれば、未知試料の磁化率を求めることができます。
質量mの試料を入れた試料管を磁気天秤へ挿入して得られた表示値をR、空の試料管を磁気天秤へ挿入して得られた表示値をR0として、比例定数kとすると以下のように示すことができます。
k(R-R0)=-(1/2) χaH20…㉓
試料の密度をd、試料の断面積をa、試料の長さをlとするとd=m/alとなります。また、χg=χ/dであるので、式㉓の右辺は以下のように変形できます。
k(R-R0)=-(1/2) χg(m/al)aH20
=-(1/2) χg(m/l)H20…㉔
式㉔をχgの形にすると以下のようになります。
χg=(l/m)(-2k/H20)(R-R0)…㉕
この-2k/H20を天秤定数Cと置けば以下のようになります。
χg=(l/m)C(R-R0)…㉖
また、ここまでの解説では試料と空気の置き換わりの補正、すなわち、空気の補正について述べていなかったので、それについても説明いたします。
空気の磁化率をχairとして式㉓に対応させると以下のようになります。
k(R-R0)=-(1/2)(χ-χair)aH20…㉗
これを、χ=の形に変形すると以下のようになります。
χ-χair=(-2k/aH20)(R-R0)=(C/a)(R-R0)
χ=(C/a)(R-R0)+χair…㉘
式㉘をχgに変形すると以下のようになります。
χg=χ/(m/al)=(l/m){C(R-R0)+aχair}…㉙
また、空気の磁化率は、xair=0.029×10-6(20℃、700mmgHg)としました。
本実験の計算において、式⑫を用いますが、計算を楽にするために、以下のように近似します。
nexp2=(3RT/NL2μB2)xmol≒8Tχmol…㉚
また、式⑭のn=の変形においては以下のようにしました。
neff2=n(n+2)
neff2+1=n2+2n+1
neff2+1=(n+1)2
√neff2+1=n+1
n=-1+√(neff2+1)…㉛
3、遷移金属錯体

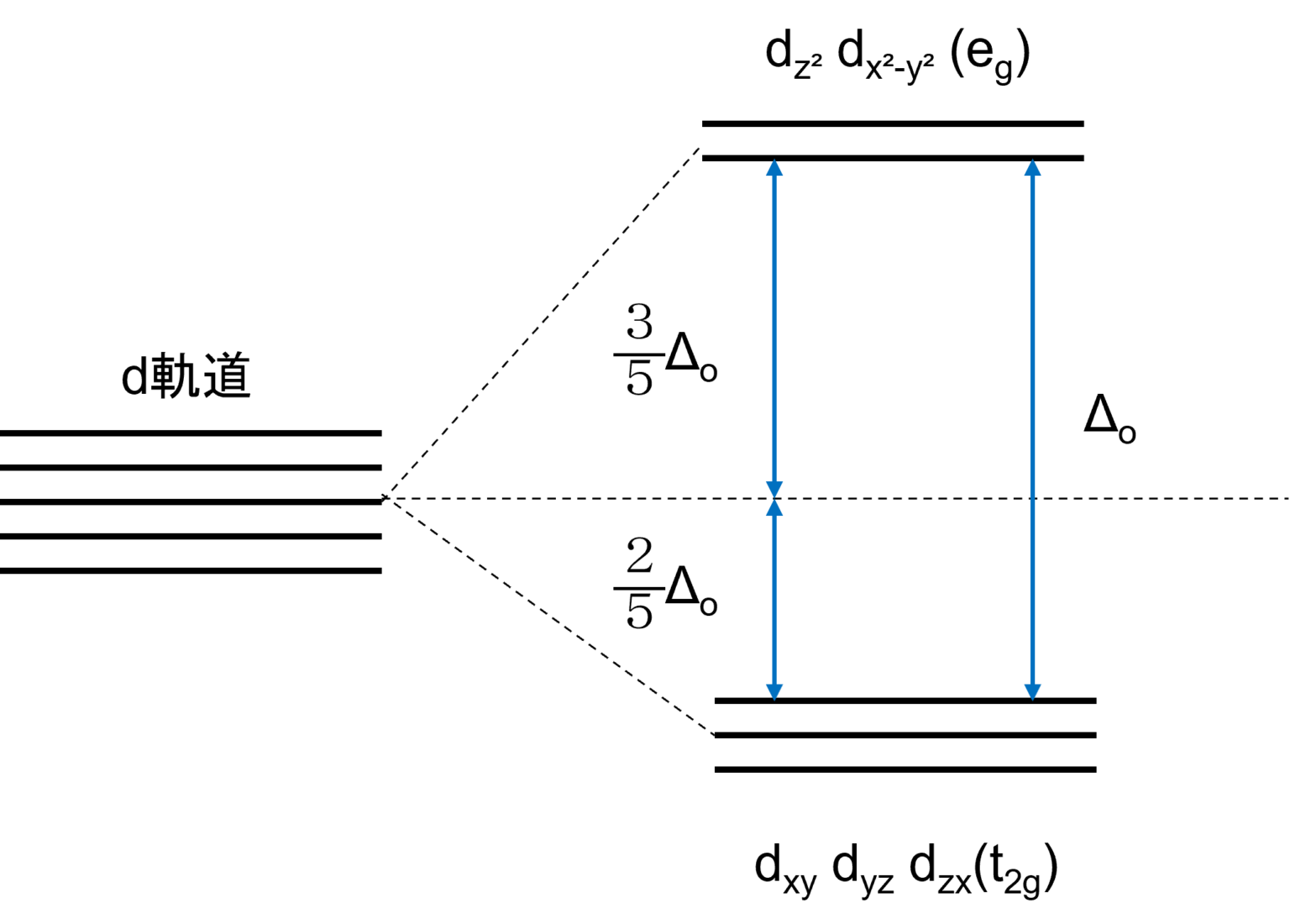
正八面体結晶場中の遷移金属イオンのd電子配置と結晶場の強さとの関係は結晶場理論を用いて説明することができます。
通常d軌道の5つは等しいエネルギーで5重に縮退しています。しかし、結晶場理論において、x軸、y軸、z軸の両端方向から6個の配位子が負の点電荷として存在し、近づいてくると考えます。
このような事を考えると軌道の形によって安定性が変わります。
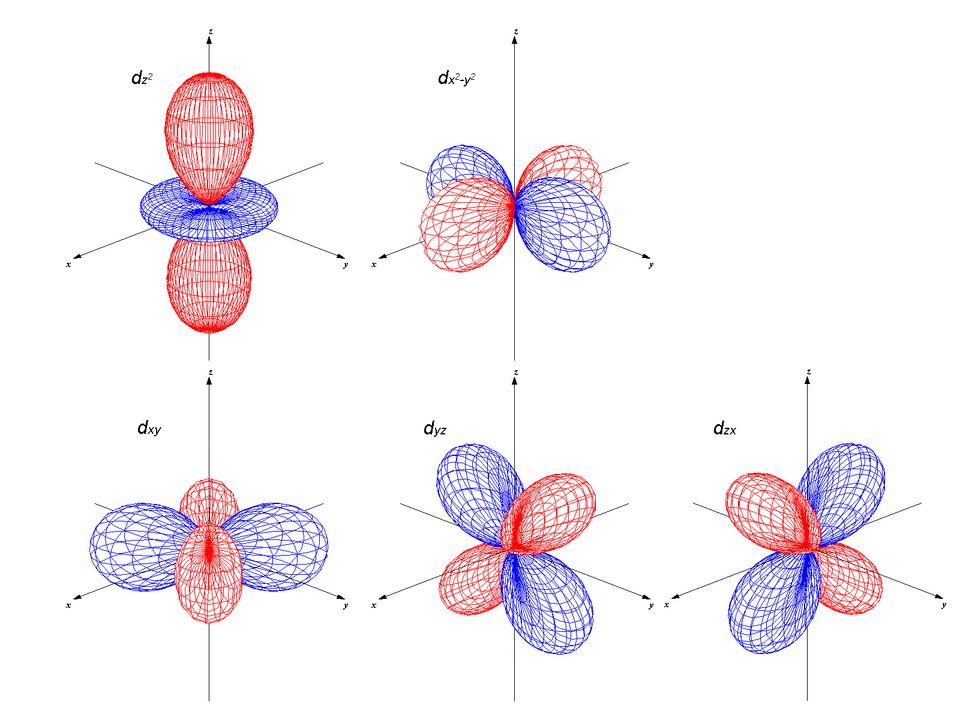
以下に、d軌道5つを示します。
ここでdz2、dx2-y2を考えると直交軸に対する配位子の方向に、電子密度が高く、電子同士が反発します。
このため、この2つの軌道はエネルギー的に不安定であることが分かります。このような2つの軌道をeg縮退軌道といいます。
一方、dzx、dyz、dxyを考えると直交軸に対する配位子の方向に、電子密度が低く、電子同士が反発しづらいです。このため、この3つの軌道はエネルギー的に安定であるといえます。このような3つの軌道をt2g縮退軌道といいます。
このような事から、正八面体結晶場中のd軌道のエネルギーは以下のように示すことができます。
このeg縮退軌道とt2g縮退軌道のエネルギーの差のことを、配位子場分裂パラメーターといいます。
また、電子の入り方としては、フント則に従い、3つまではt2g縮退軌道に入ります。問題は、4つ目以降の電子であって、これは配位子の分光化学系列によって決められます。
分光化学系列が大きいと配位子場分裂パラメーターが大きくなり、そのためt2g縮退軌道に入って低スピン錯体になります。一方、分光化学系列が小さいと配位子場分裂パラメーターが小さくなり、そのためeg縮退軌道に入った方が電子同士のスピン生成エネルギーよりも安定であるため、高スピン錯体になります。
4、~まとめ~
いかがでしたか?
今回は、遷移金属錯体の磁化率を測定し、特性を確認する実験について、磁化率,測定方法,遷移金属錯体という3つのキーワードから説明しました。どの章も重要なのでしっかりと抑えておきましょう。
また、参考文献は以下の通りになります。
1、日本化学会編,新実験化学講座3基礎技術2,丸善(1976),p.43~76
最後になりますが、参考文献以外はコピペ厳禁です。バレます。気を付けてください。自分で理解してまとめてください。
また、完全に情報を網羅しきれていないと思いますので、質問等ありましたら、下のコメント欄にコメントお願いします。
今回の記事は以上になります。最後まで読んでいただき、ありがとうございました。
 引用:
引用: